Xét cân bằng: N2O4(k) D 2NO2(k) ở 250C.
Khi chuyển dịch sang một trạng thái cân bằng mới nếu nồng độ của N2O4 tăng lên 9 lần thì nồng độ của NO2 thay đối:
A. tăng 9 lần.
B. giảm 3 lần.
C. tăng 4,5 lần.
D. tăng 3 lần.
Xét cân bằng: N2O4(k) D 2NO2(k) ở 250C.
Khi chuyển dịch sang một trạng thái cân bằng mới nếu nồng độ của N2O4 tăng lên 9 lần thì nồng độ của NO2 thay đối:
A. tăng 9 lần.
B. giảm 3 lần.
C. tăng 4,5 lần.
D. tăng 3 lần.
Đáp án D
Hằng số cân bằng: K c = [ NO 2 ] 2 [ N 2 O 4 ]
Khi tăng nồng độ N2O4 lên 9 lần đê’hằng số K không đổi thì nồng độ NO2 phải tăng lên 3 lần.
Xét cân bằng: N2O4 (k) ⇄ 2NO2 (k) ở 25oC.
Khi chuyển dịch sang một trạng thái cân bằng mới nếu nồng độ của N2O4 tăng lên 9 lần thì nồng độ của NO2
A. tăng 9 lần.
B. tăng 3 lần.
C. tăng 4,5 lần.
D. giảm 3 lần.
Chọn đáp án B
Gọi nồng độ của N2O4 và NO2 ban đầu lần lượt là a, x.
Sau khi tăng nồng độ của N2O4 là 9a, của NO2 là y: nên
![]()
Xét cân bằng: N 2 O 4 ( k ) ⇄ 2 N O 2 ( k ) ở 25 o C . Khi chuyển dịch sang một trạng thái cân bằng mới nếu nồng độ của N 2 O 4 tăng lên 9 lần thì nồng độ của N O 2
A. tăng 9 lần
B. tăng 3 lần
C. tăng 4,5 lần
D. giảm 3 lần
Chọn B
Chuyển dịch sang một trạng thái cân bằng mới, nhiệt độ không đổi → Kc không đổi.
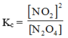
→ nồng độ của N 2 O 4 tăng lên 9 lần thì nồng độ của N O 2 tăng 3 lần
Xét cân bằng. N2O4 (k) ⇆ 2NO2 (k) ở 25oC. Khi chuyển dịch sang một trạng thái cân bằng mới nếu tăng nồng độ của N2O4 lên 9 lần thì nồng độ của NO2
A. tăng 9 lần.
B. tăng 3 lần.
C. tăng 4,5 lần.
D. giảm 3 lần
Đáp án B.
Vt = k[N2O4], Vn = k[NO2]2
ở trạng thái cân bằng. Vt = Vn
Nên khi tăng nồng độ của N2O4 lên 9 lần thì nồng độ của NO2 tăng 3 lần
Phản ứng hoá học sau đã đạt trạng thái cân bằng :
2 NO 2 ↔ N 2 O 4 △ H < 0
Cân bằng hoá học sẽ chuyển dịch theo chiều nào khi tăng nhiệt độ ?
Khi tăng nhiệt độ, cân bằng hoá học của phản ứng sẽ chuyển sang chiều nghịch. Bởi vì phản ứng thuận toả nhiệt
Cho các cân bằng hóa học sau:
(a) 2HI + Cl2 (k) → 2HCl + I2 (k)
(b) 2NO2(k) → N2O4(k)
(c) 3H2 + N2(k) → 2NHH2 (k)
(d) 2SO2 + O2 → 2SO2(k)
Ở nhiệt độ không đổi, khi thay đổi áp suất chung của mỗi hệ cân bằng, cân bằng nào ở trên không bị chuyển dịch:
A. (a).
B. (b).
C. (c).
D. (d).
Chọn A.
Khi áp suất thay đổi các phản ứng nào có tổng số mol khí ở hai vế phương trình khác nhau sẽ bị chuyển dịch: (b), (c), (d).
Cho các cân bằng hóa học sau:
(a) H2 (k) + I2 (k) ![]() 2HI (k).
2HI (k).
(b) 2NO2 (k) ![]() N2O4 (k)
N2O4 (k)
(c) 3H2 + N2 (k) ![]() 2NH3 (k)
2NH3 (k)
(d) 2SO2 (k) + O2 (k) ![]() 2SO3 (k)
2SO3 (k)
Ở nhiệt độ không đổi, khi thay đổi áp suất chung của mỗi hệ cân bằng, cân bằng hóa học nào ở trên không bị chuyển dịch?
A. d
B. b
C. c
D. a
Đáp án : D
Nếu hệ số các chất khí 2 vế bằng nhau thì cân bằng không chịu sự ảnh hưởng do thay đổi áp suất chung của hệ
Cho các cân bằng hóa học sau:
(a) 2 HI ( k ) + Cl 2 ( k ) ⇄ 2 HCl ( k ) + I 2 ( k )
(b) 2 NO 2 ( k ) ⇄ N 2 O 4 ( k )
(c) 3 H 2 ( k ) + N 2 ( k ) ⇄ 2 NH 2 ( k )
(d) 2 SO 2 ( k ) + O 2 ( k ) ⇄ 2 SO 3 ( k )
Ở nhiệt độ không đổi, khi thay đổi áp suất chung của mỗi hệ cân bằng, cân bằng nào ở trên không bị chuyển dịch:
A. (c).
B. (b).
C. (a).
D. (d).
Chọn đáp án A
Khi áp suất thay đổi các phản ứng nào có tổng số mol khí ở hai vế phương trình khác nhau sẽ bị chuyển dịch.Gồm : (b) (c) (d)
Cho các cân bằng hóa học sau:
( a ) H 2 ( k ) + I 2 ( k ) ⇌ 2 HI ( k ) ( b ) 2 NO 2 ( k ) ⇌ N 2 O 4 ( k ) ( c ) N 2 ( k ) + 3 H 2 ( k ) ⇌ 2 NH 3 ( k ) ( d ) 2 SO 2 ( k ) + O 2 ( k ) ⇌ 2 SO 3 ( k )
Ở nhiệt độ không đổi, khi thay đổi áp suất chung của mỗi hệ cân bằng, cân bằng hóa học nào ở trên không bị chuyển dịch?
A. (a).
B. (c).
C. (b).
D. (d).
Đáp án A
Cân bằng hóa học không bị chuyển dịch khi thay đổi áp suất chung của hệ là:
( a ) H 2 ( k ) + I 2 ( k ) ⇌ 2 HI ( k )